三抗能复制双抗的“神话”吗?
9月下旬,泽璟制药的注射用ZG006(一款靶向CD3/DLL3/DLL3的三特异性抗体)登记启动III期临床研究,用于治疗复发性小细胞肺癌——由此ZG006成为全球首个进入III期的肿瘤三抗。
前后脚,一场震动行业的收购案落定:丹麦Genmab以约80亿美元将荷兰公司Merus收入囊中,交易金额刷新了欧洲生物科技领域的高额收购纪录。
被收购的Merus,除了颇受关注的双抗在研管线,赋予其想象空间的还有公司专有的三抗平台Triclonics®。一年半前,正是这一平台帮助Merus斩获与吉利德总额超15亿美金的合作。
几家公司以截然不同的方式,将“三特异性抗体”这一前沿技术再度推向了行业聚光灯下。
凭借多一个靶点结合位点的结构优势,三抗旨在实现更强的靶向特异性、更优的临床疗效与更低的脱靶毒性,从而被视为下一代免疫疗法的重点方向。
不仅国内外企业都在积极参与研发,全球在研项目突破百个,艾伯维、默沙东等跨国巨头更在近年来以数十亿美元的密集交易为其潜力“投票”,一场关于未来治疗格局的新角逐正在进行。
一个核心问题随之浮现:在双抗成功开辟的道路上,能够同时靶向三个靶点的三抗,是简单的技术叠加,还是足以复制甚至超越前者的范式革命?
当康方生物凭借AK104和AK112两款双抗药物的贡献,从市值不足100亿港元的“小透明”成长为突破1000亿港元的“小巨头”,未来,三抗企业又能否复制康方生物的“神话”?
TONACEA01三抗站上新风口
单抗药物因其特异性强、靶向性高和毒副作用小等特点,已在肿瘤、自身性免疫疾病等领域广泛应用。
但是,由于疾病的复杂性,例如在肿瘤治疗领域,由于免疫抑制性微环境及肿瘤免疫逃逸机制的复杂性,这种针对单一靶点的药物往往难以达到理想的治疗效果,临床上表现为响应率不高,获益群体比较有限。
双抗药物应运而生,为治疗提供了新途径。目前全球已有多款双抗药物获批上市,适应症主要集中在肿瘤领域。
然而,作为“敌人”的癌细胞不会坐以待毙,其在治疗过程中往往会展现出狡猾本性,改变表面抗原的表达模式,避开双抗的识别,并主动构建各种“防御工事”来抵抗免疫系统的攻击。
因此,科学家开始深入思考:能否设计出更加智能和坚固的"桥梁",让它不仅能够同时识别敌人的多种伪装,还能够招募不同类型的友军,形成更加全面和持久的包围攻势?
在此驱动下,可以同时靶向三种不同的靶抗原或标志物的三抗,成为下一代免疫疗法研发的核心焦点。
与双抗相比,三抗还能够与肿瘤细胞或免疫细胞表面的另一个靶点相结合,或桥接免疫细胞并阻断双信号通路等作用,更有利于将药物或免疫细胞重定向至肿瘤部位,增强结合特异性,提高靶向性,降低脱靶毒性,从而提升抗肿瘤能力。
以泽璟制药开发的ZG006为例,结合两个不同表位的DLL3,通过靶向DLL3和CD3将肿瘤细胞和T细胞结合,用于T细胞介导的肿瘤细胞杀伤,对于DLL3不同表达量的肿瘤细胞均有较好的杀伤效果。
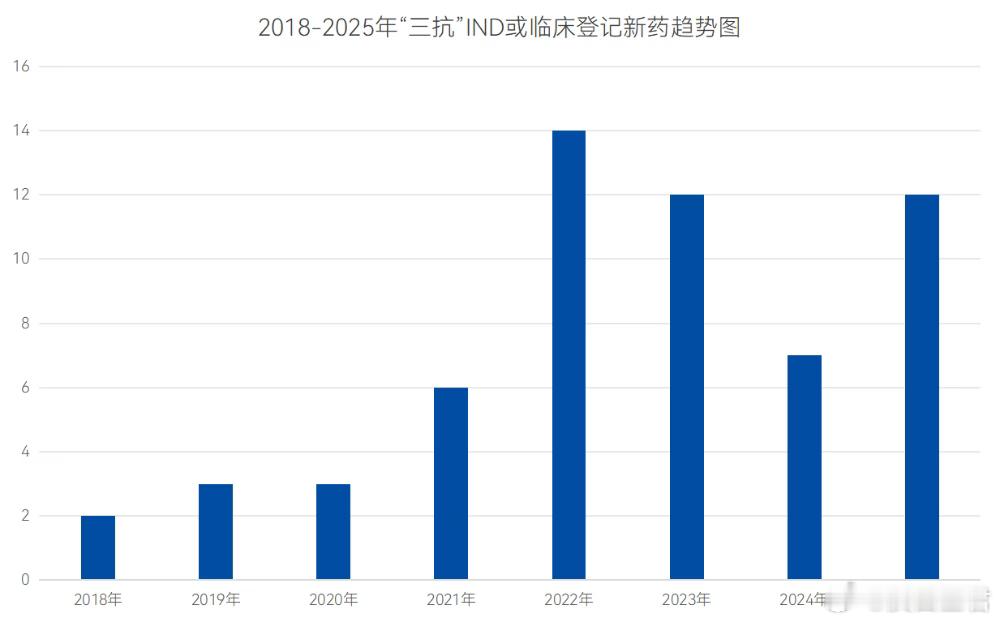
近十年来,三抗从概念验证快速步入临床研究,已有多家生物医药企业布局。不完全数据统计,在研三抗产品已突破100个,大多数项目处于临床早期阶段,适应症主要集中在肿瘤和眼科疾病,尤其是肿瘤领域。
来源:药智数据
作用靶点上,在研三抗作用靶点比较多样,主要集中在CD3、PD-L1、BCMA、VEGF等,其中CD3靶点最热门。从靶点组合来看,GPRC5D/BCMA/CD3、PD-L1/VEGF/TGF-β相对热门,且在研药物进展较快。
TONACEA02BD交易潜力初现
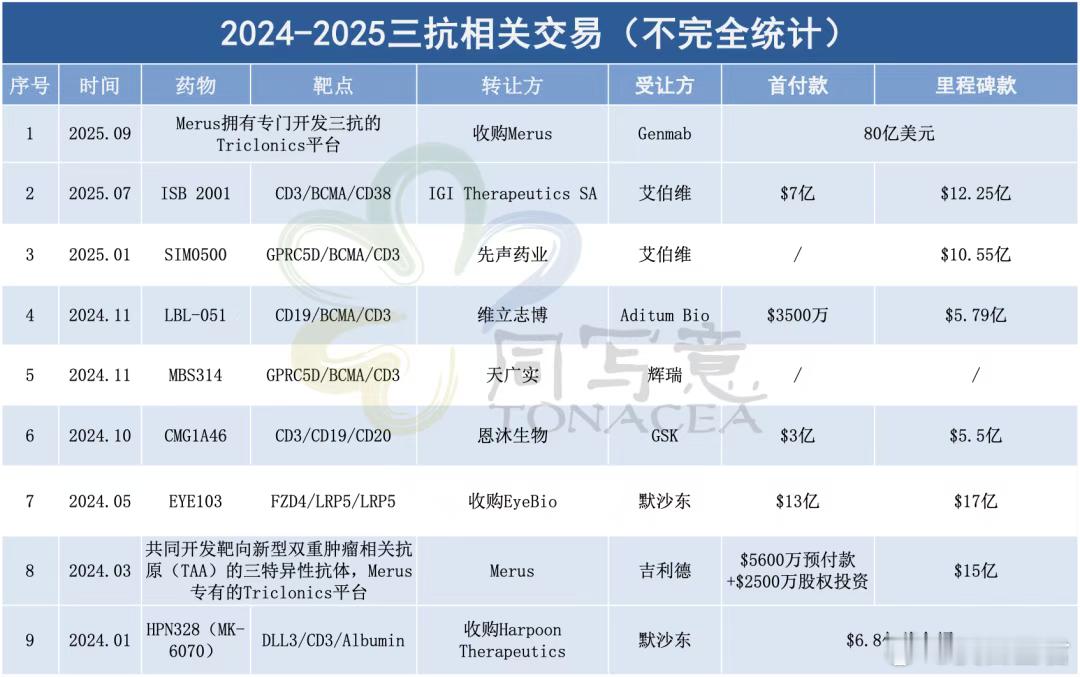
虽然目前未有三抗获批上市,但其潜力已引发国内外药企关注,并促使达成多项交易,不乏MNC的身影。
2025年,艾伯维先后就有两笔出手:先是1月,以10.55亿美元引进先声药业GPRC5D/BCMA/CD3三抗SIM0500;紧接着半年后的7月,豪掷将近20亿美金,拿下IGI主要资产CD3/CD38/BCMA三抗TCE ISB 2001,在北美、欧洲、日本和大中华区开发、制造和商业化的独家权利。
连续引进两款TCE三抗产品,可见艾伯维对多特异性抗体药物的态度改变以及行业技术迭代加速的信号。其首席执行官Rob Michael也曾在6月高盛的一次活动上表示,将多特异性抗体作为公司肿瘤领域交易的重点。
相比艾伯维通过BD引进潜力重磅品种,补足其在血液瘤领域的优势,默沙东的收购要来得更早且更加猛烈。
2024年5月,默沙东将以13亿美元的前期付款和高达17亿美元的未来里程碑付款收购EyeBio公司。 EyeBio的先导候选药物Restoret(EYE103)是一种在研的、潜在的“first-in-class”的四价、三特异性Wnt抗体,旨在解决视网膜疾病患者未满足的医疗需求。Restoret通过玻璃体内注射给药,旨在通过激动Wnt途径消除视网膜血管疾病中的渗漏,恢复和维持血-视网膜屏障(BRB)。
在这之前,2024年1月,默沙东还以约6.8亿美元收购了Harpoon Therapeutics,后者的核心管线HPN328(MK-6070)为一款DLL3/CD3/Albumin三特异性抗体。7个月后,第一三共和默沙东宣布将共同开发及商业化MK-6070,默沙东仅保留了日本权益。
当然,近两年,出手三抗的MNC除了艾伯维、默沙东,还有吉利德、GSK、辉瑞。
吉利德于2024年3月与Merus达成一项研究合作许可协议,共同开发靶向新型双重肿瘤相关抗原(TAA)的三抗;GSK在同年10月和恩沐生物达成合作,以3亿美元的首付款从恩沐生物收购CMG1A46;辉瑞则紧随其后,在11月与天广实达成GPRC5D/BCMA/CD3三抗MBS314共同开发合作。
还值得注意的是,去年11月,维立志博与风险投资公司Aditum Bio达成了NewCo交易,基于维立志博全球首创CD19xBCMAxCD3三抗TCE抗体LBL-051成立新药研发公司Oblenio Bio,并达成了独家选择权及许可协议。
Aditum为Oblenio提供资金,双方合作推进LBL-051进入临床,Oblenio拥有全球范围内开发、生产和商业化LBL-051的独家选择权和许可,维立志博则获得3500万美元的首付款和近期付款,在达成开发、监管注册、销售里程碑事件后,维立志博还将有权获得最高达5.79亿美元的总交易额款项,以及未来产品的销售分成。此外,维立志博还将有权获得Oblenio的股权。
可以看到,在海外巨头这一轮轰轰烈烈的”扫货“中,恩沐生物、先声药业、天广实、维立志博的三抗产品,凭借其差异化的优势受到青睐,成功出海。
TONACEA03下一个BD爆点?
除了以上交易涉及的产品,随着PD-1/VEGF的靶点组合已在临床上得到验证,且拥有超越PD-1的潜力,针对PD-1/VEGF靶点组合延伸出来的三抗靶点,有望成为引爆市场的下一个风口。
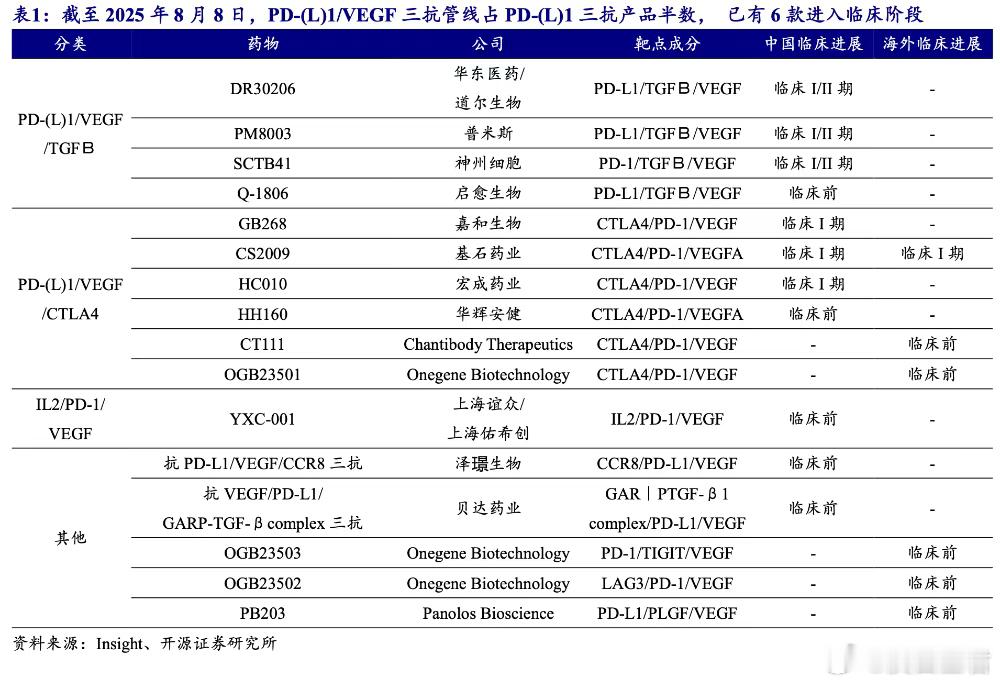
根据开源证券的统计,截至2025年8月8日,全球共有32款处于临床及临床前PD-(L)1三抗(项目状态积极),其中16款为PD-(L)1/VEGF三抗药物。
从迭代逻辑来看,现有的PD-(L)1/VEGF双抗PFS获益显著,但总生存期获益仍需进一步明确。而三抗的升级,正是希望在这一方面做更多努力。
目前全球药企的核心思路,是叠加一些已经被验证,或者机制相对清晰的靶点,因而在多种PD-(L)1/VEGF三抗中,PD-(L)1/VEGF/TGFβ三抗及PD-(L)1/VEGF/CTLA-4三抗是最早进入临床阶段的两类多抗。
例如华东医药DR30206,临床前数据显示,在肺癌小鼠模型中,高剂量(25mg/kg)DR30206 比低剂量肿瘤抑制效果更佳,且DR30206 所有剂量组均比Atezolizumab(5mg/kg)联合或不联合Bevacizumab(5mg/kg)组治疗效果更显著。
R30206已在中国开展两项临床,分别为DR30206单药(1mg/kg~30mg/kg Q2W/Q3W)治疗多种实体瘤及DR30206(15/20mg/kg Q2W、30mg/kg Q3W)联合化疗一/二线治疗胃癌、食管腺癌和结直肠癌。
还有基石药业CS2009,已于2024年12月开展中国/澳大利亚首个I/II临床试验,预计年底前入组超100例患者。截至基石药业公告日,CS2009 在所有已评估的剂量水平上展现出良好的耐受性,并且已在低剂量组的“冷肿瘤”及PD-(L)1 经治患者中观察到抗肿瘤活性。
除了上述产品,PD-(L)1/VEGF 双抗和 PD-(L)1/IL-2 双抗的显著进展验证了 PD-(L)1 与 VEGF和 IL-2 的疗效协同性,作为将这两个具有明确协同效应的靶点同时整合的三抗药物,PD-(L)1/VEGF/IL-2 也颇受关注,目前仅有一款(上海谊众)处于临床前阶段。
上海谊众YXC-001有望于2025年内完成国内与国际的IND同步申报。YXC-001临床前初步药效试验显示,该多功能抗体能够多靶点协同发挥作用,对比帕博利珠单抗等单抗及双抗类药物,具有抑制肿瘤优势。
几款重点产品,谁能率先在临床端带来新突破,并刷新国产创新药出海记录?拭目以待。
— 结语—
整体来看,三抗的发展仍处于相对早期,研发并不容易,靶点叠加并不直接等同于效果提高,也绝不是简单的排列组合,复杂性远超预期。
有人如是比喻:如果把传统单抗比作制造一把简单而可靠的工具,那么三抗就像是要制造一台能够同时执行三种不同任务的精密设备——这种复杂性的提升带来了前所未有的技术挑战。
三抗的征途,也绝非简单复制双抗的路径。
它以其内在的复杂性与灵活性,呈现出三大趋势:纵向的技术迭代,向着四特异性抗体等更复杂形式演进;横向的适应症扩展,从肿瘤迈向自免、感染等更广阔疾病领域;以及深度的联合疗法探索(如三抗+ADC),旨在构建协同作战的“组合拳”。
当科学的探索从“能否实现”迈向“如何整合”,三抗的故事,才真正进入了最激动人心的章节。